Abstract
Background
In comparison to normal brain tissue, glioblastomas exhibit significantly increased glucose uptake. Brain edema is a common complication during adjuvant chemoradiotherapy, leading to a requirement for glucocorticoid treatment. Glucocorticoid treatment frequently causes considerable deregulation of blood glucose levels. Therefore, episodes of hyperglycemia may contribute to radio- and/or chemoresistance.
Patients and methods
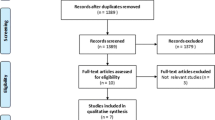
This study comprises a retrospective analysis of the influence of hyperglycemic episodes (HEs) during adjuvant therapy on the overall survival of 106 glioblastoma multiforme patients.
Results
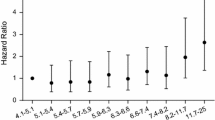
The occurrence of one or more deregulated blood glucose value(s) > 10 mM is associated with a reduction in median overall survival from 16.7 to 8.8 months. A significantly poorer overall survival of patients with hyperglycemia could also be detected in subgroup analyses of patients with complete tumor resection and complete treatment according to the EORTC 22891/26891 trial protocol, as well as in a multivariate Cox proportional hazards analysis. A history of diabetes mellitus had no influence on prognosis.
Discussion
Our data suggest that the observed negative impact of elevated blood glucose levels on overall survival may not solely be explained by the patients’ poorer general condition; the elevated blood glucose concentration itself may play a pathogenetic role. This could be due to increased activity of antioxidant systems, elevated expression of DNA damage response proteins and protection of hypoxic tumor cells against apoptosis combined with hypoxia-mediated radioresistance.
Conclusion
A possible prognostic impact of elevated blood glucose levels during the period of adjuvant (chemo-) radiotherapy of glioblastoma should be evaluated in a prospective clinical trial.
Zusammenfassung
Hintergrund
Glioblastome zeigen im Vergleich mit normalem Gehirngewebe eine deutlich vermehrte Glukoseaufnahme. Im Rahmen der adjuvanten Radio(chemo)therapie von Glioblastomen treten vielfach Hirnödeme auf, die eine Glukokortikoidgabe erforderlich machen. Hierdurch kommt es häufig zu nicht unerheblichen Blutzuckerentgleisungen. Es stellt sich die Frage, ob Hyperglykämieepisoden während der adjuvanten Therapie zu einer Radio- und/oder Chemoresistenz beitragen können.
Patienten und Methoden
Die Studie analysiert retrospektiv den Einfluss von Hyperglykämieepisoden während der adjuvanten Therapie auf das Gesamtüberleben von 106 Patienten mit Glioblastoma multiforme.
Ergebnisse
Das Auftreten von einer oder mehreren Entgleisungen des Blutzuckers mit Werten > 10 mM war mit einer Verminderung des medianen Gesamtüberlebens von 16,7 Monaten auf 8,8 Monate verbunden. Ein signifikant schlechteres Gesamtüberleben von Patienten mit Blutzuckerentgleisungen ließ sich auch in Subgruppenanalysen von vollständig resezierten und vollständig nach EORTC-22891/26891-Protokoll therapierten Patienten sowie in einer multivariaten Cox-Analyse (Cox proportional hazards) nachweisen. Ein manifester Diabetes mellitus als Vorerkrankung hatte keinen Einfluss auf die Prognose.
Diskussion
Unsere Daten weisen darauf hin, dass der beobachtete negative Einfluss erhöhter Blutglukosekonzentrationen auf das Gesamtüberleben möglicherweise nicht allein mit einem schlechteren Allgemeinzustand der Patienten zu erklären ist und der Hyperglykämie selbst somit eine pathogenetische Bedeutung zukäme. Dies könnte in einer erhöhten Aktivität antioxidativer Systeme, gesteigerter Expression von Proteinen der DNA-Schadensantwort und in einem Schutz hypoxischer Tumorzellen vor Apoptose bei gleichzeitig erhöhter hypoxiebedingter Radioresistenz begründet sein.
Schlussfolgerung
Ein möglicher prognostischer Einfluss von Blutzuckerentgleisungen während der Phase der adjuvanten Radio(chemo)therapie sollte in einer prospektiven klinischen Studie untersucht werden.


Similar content being viewed by others
References
Bonuccelli G, Tsirigos A, Whitaker-Menezes D et al (2010) Ketones and lactate “fuel” tumor growth and metastasis: evidence that epithelial cancer cells use oxidative mitochondrial metabolism. Cell Cycle 9:3506–3514
Curran WJ Jr., Scott CB, Horton J et al (1993) Recursive partitioning analysis of prognostic factors in three Radiation Therapy Oncology Group malignant glioma trials. J Natl Cancer Inst 85:704–710
Derr RL, Ye X, Islas MU et al (2009) Association between hyperglycemia and survival in patients with newly diagnosed glioblastoma. J Clin Oncol 27:1082–1086
Jelluma N, Yang X, Stokoe D et al (2006) Glucose withdrawal induces oxidative stress followed by apoptosis in glioblastoma cells but not in normal human astrocytes. Mol Cancer Res 4:319–330
Li J, Ayene R, Ward KM et al (2009) Glucose deprivation increases nuclear DNA repair protein Ku and resistance to radiation induced oxidative stress in human cancer cells. Cell Biochem Funct 27:93–101
Mayer A, Schneider F, Vaupel P et al (2012) Differential expression of HIF-1 in glioblastoma multiforme and anaplastic astrocytoma. Int J Oncol 41:1260–1270
McGirt MJ, Chaichana KL, Gathinji M et al (2008) Persistent outpatient hyperglycemia is independently associated with decreased survival after primary resection of malignant brain astrocytomas. Neurosurgery 63:286–291; discussion 291
Mergenthaler P, Lindauer U, Dienel GA et al (2013) Sugar for the brain: the role of glucose in physiological and pathological brain function. Trends Neurosci 36:587–597
Oudard S, Arvelo F, Miccoli L et al (1996) High glycolysis in gliomas despite low hexokinase transcription and activity correlated to chromosome 10 loss. Br J Cancer 74:839–845
Sahm F, Capper D, Jeibmann A et al (2012) Addressing diffuse glioma as a systemic brain disease with single-cell analysis. Arch Neurol 69:523–526
Sattler UG, Meyer SS, Quennet V et al (2010) Glycolytic metabolism and tumour response to fractionated irradiation. Radiother Oncol 94:102–109
Stupp R, Mason WP, van den Bent MJ et al (2005) Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med 352:987–996
Vaupel P (2004) Tumor microenvironmental physiology and its implications for radiation oncology. Semin Radiat Oncol 14:198–206
Vaupel P, Kallinowski F, Okunieff P (1989) Blood flow, oxygen and nutrient supply, and metabolic microenvironment of human tumors: a review. Cancer Res 49:6449–6465
Warburg O, Posener K, Negelein E (1924) Über den Stoffwechsel der Carcinomzelle. Biochem. Zeitschr. 152:309–344
Yamamori T, Meike S, Nagane M et al (2013) ER stress suppresses DNA double-strand break repair and sensitizes tumor cells to ionizing radiation by stimulating proteasomal degradation of Rad51. FEBS Lett 587:3348–3353
Yuan S, Wang F, Chen G et al (2013) Effective elimination of cancer stem cells by a novel drug combination strategy. Stem Cells 31:23–34
Acknowledgements
The authors thank Erika Budo-Guetaifi for careful evaluation of patient data and Dr. Debra Kelleher for her valuable editorial help during preparation of this manuscript.
Conflict of interest
A. Mayer, P. Vaupel, H.-G. Struss, A. Giese, M. Stockinger and H. Schmidberger state that there are no conflicts of interest. The accompanying manuscript does not include studies on humans or animals.
Author information
Authors and Affiliations
Corresponding author
Rights and permissions
About this article
Cite this article
Mayer, A., Vaupel, P., Struss, HG. et al. Strong adverse prognostic impact of hyperglycemic episodes during adjuvant chemoradiotherapy of glioblastoma multiforme. Strahlenther Onkol 190, 933–938 (2014). https://doi.org/10.1007/s00066-014-0696-z
Received:
Accepted:
Published:
Issue Date:
DOI: https://doi.org/10.1007/s00066-014-0696-z